Questão 1
(UFC-CE-mod.) Ao desejar identificar o conteúdo de um cilindro contendo um gás monoatômico puro, um estudante de Química coletou uma amostra desse gás e determinou sua densidade, d=5,38 g/L, nas seguintes condições de temperatura e pressão: 15ºC e 0,97atm. Com base nessas informações, e assumindo o modelo do gás ideal, calcule a a massa molar do gás .
Dado: R = 0,082 atm.L. mol-1 . K-1; T(K) = 273,15 + T(ºC)
a) 1,310 g . mol-1.
a) 6,81 g . mol-1.
b) 13,10 g . mol-1.
c) 124,23 g . mol-1.
d) 131,05 g . mol-1.
e) 165,04 g . mol-1.
Questão 2
(Unicentro-PR) Um profissional da área ambiental recebeu uma amostra de gás, sem identificação, para análise. Após algumas medidas, ele obteve os seguintes dados:
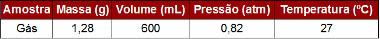
Tabela em exercício sobre equação de Clapeyron
Com base nos valores obtidos, entre os gases indicados nas alternativas, conclui-se que a amostra era de:
a) O2.
b) O3.
c) N2.
d) SO2.
e) H2.
Dados: O = 16 u, H = 1 u, N = 14 u, S = 32 u; R = 0,082 atm.L. mol-1 . K-1.
Questão 3
Determine o volume ocupado por 1 mol de substância gasosa a 10 atm de pressão e 25ºC.
a) 22,4 L.
b) 2,44 L.
c) 20,5 L.
d) 0,205 L.
e) 244,36 L
Questão 4
Calcule a pressão total de uma mistura gasosa formada por 3 mol de um gás A e 2 mol de um gás B, considerando que a temperatura final é de 300 K e o volume é de 15 L.
a) 8,2 atm.
b) 3,28 atm.
c) 4,92 atm.
d) 9,84 atm.
e) 1,84 atm.
Resposta Questão 1
Alternativa “d”.
Considerando o volume de 1 L de gás, sua massa é de 5,38 g (uma vez que a densidade é 5,38 g/L). Lembrando também que a temperatura deve ser dada na escala absoluta, temos: T(K) = 273,15 + T(ºC) → T(K) = 273,15 + 15 ºC → T(K) = 288,15 K.
Portanto, podemos aplicar a equação de estado dos gases:
P . V = n . R . T
P . V = m . R . T
M
M = m . R . T
P . V
M = (5,38 g) . (0,082 atm.L. mol-1 . K-1) . (288,15 K)
(0,97atm) . (1 L)
M = 131,05 g . mol-1
Resposta Questão 2
Alternativa “d”.
Dados:
m = 1,28 g;
V = 600 mL = 0,6 L;
T = 27 ºC = 300 K;
R = 0,082 atm.L. mol-1 . K-1.
P = 0,82 atm;
M= ?
Vamos usar a equação de Clapeyron para descobrir a massa molar do gás e determinar sua natureza:
P . V = n . R . T
P . V = m . R . T
M
M = m . R . T
P . V
M = (1,28 g) . (0,082 atm.L. mol-1 . K-1) . (300 K)
(0,82atm) . (0,6 L)
M = 64 g . mol-1
Esse é o valor da massa molar do SO2.
Resposta Questão 3
Alternativa “b”.
Dados:
n = 1 mol;
V = ?
T = 25 ºC = 298 K;
R = 0,082 atm.L. mol-1 . K-1.
P = 10 atm;
Usando a equação de estado dos gases, temos:
P . V = n . R . T
V = n . R . T
P
V = (1 mol) . (0,082 atm.L. mol-1 . K-1) . (298 K)
(10 atm)
V = 2,44 L
Resposta Questão 4
Alternativa “a”.
Usando a equação de estado dos gases, temos:
P . V = n . R . T
P = n . R . T
V
P = (5 mol) . (0,082 atm.L. mol-1 . K-1) . (300 K)
(15 L)
P = 8,2 atm



