Questão 1
(ITA-SP) Na figura a seguir, o balão A contém 1 litro de solução aquosa 0,2 mol/L em KBr, enquanto o balão B contém 1 litro de solução aquosa 0,1 mol/L de FeBr3. Os dois balões são mantidos na temperatura de 25°C. Após a introdução das soluções aquosas de KBr e de FeBr3 as torneiras TA e TB são fechadas, sendo aberta a seguir a torneira TC.
As seguintes afirmações são feitas a respeito do que será observado após o estabelecimento do equilíbrio.
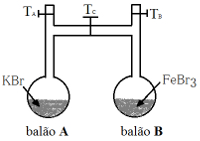
Exercício sobre pressão osmótica
I - A pressão osmótica das duas soluções será a mesma.
II - A pressão de vapor da água será igual nos dois.
III - O nível do líquido no balão A será maior do que o inicial.
IV - A concentração da solução aquosa de FeBr3 no balão B será maior do que a inicial.
V - A molaridade do KBr na solução do balão A será igual à molaridade de FeBr3 no balão B.
Qual das opções a seguir contém apenas as afirmações corretas?
a) I e II.
b) I, III e IV.
c) I, IV e V.
d) II e III.
e) II, III, IV e V.
Questão 2
(UFRS) Através da pressão osmótica não se pode explicar:
a) o tingimento de roupas com corantes orgânicos.
b) a injeção de soro fisiológico isotônico na corrente sanguínea.
c) a conservação de carne com sal (charque, por exemplo).
d) o transporte de seiva das raízes até as folhas das plantas.
e) a dificuldade de adaptação de peixes marinhos em água doce.
Questão 3
Considere as seguintes soluções aquosas:
I – 0,1 mol/L de sacarose;
II – 0,2 mol/L de sacarose;
III – 0,1 mol/L de ácido clorídrico (HCl);
IV – 0,2 mol/L de ácido clorídrico (HCl);
V – 0,1 mol/L de hidróxido de sódio (NaOH).
Considerando que o ácido clorídrico esteja totalmente ionizado nas soluções III e IV, que o hidróxido de sódio esteja dissociado completamente na solução V e que todas as soluções estejam à mesma temperatura, assinale a alternativa que as coloca corretamente em ordem crescente de pressão osmótica:
a) IV < II = V = III < I.
b) I < II = III = V < IV.
c) IV < II < V < III < I.
d) IV < V = III = II < I.
e) VI < II < III < IV< V.
Questão 4
Na aparelhagem da figura a seguir, para impedir a osmose, seria necessário aplicar sobre o anteparo uma pressão igual a:
a) 2,8 atm.
b) 5,6 atm.
c) 11,2 atm.
d) 22,4 atm.
e) 44,8 atm
(Dado: R = 0,082 atm . L . K-1 . Mol-1).
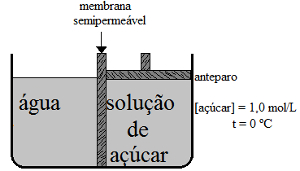
Aparelhagem em exercício sobre pressão osmótica
Resposta Questão 1
Alternativa “a”.
O efeito coligativo depende do produto M . i (número de partículas em concentração mol/L).
KBr → K+ + Br-
↓ ↓ ↓
1 mol 1 mol 1 mol
1 mol/L 2 mol/L
FeBr3 → Fe3+ + 3 Br-
↓ ↓ ↓
1 mol 1 mol 3 mol
1 mol/L 4 mol/L
1 mol/L de KBr produz, na verdade, 2 mol/L de partículas, enquanto 1 mol/L de FeBr3 produz 4 mol/L de partículas. Esses são os valores de i (fator de Van't Hoff). Agora calculando o produto M . i, temos:
KBr: M . i = 0,2 mol/L . 2 = 0,4 mol/L
FeBr3: M . i = 0,1 mol/L . 4 = 0,4 mol/L
Como o número de partículas em mol/L é o mesmo, temos que a afirmação I está correta, pois a pressão osmótica das duas soluções é a mesma. Além disso, a pressão de vapor da água é igual nos dois balões, mostrando que a alternativa II também está correta.
Resposta Questão 3
Alternativa “b”.
Vamos determinar a relação das pressões osmóticas (π) das soluções acima, considerando que a constante universal dos gases (R) e a temperatura não interferem, pois são as mesmas para todos os casos:
I. Sacarose 0,1 mol/L – molecular, não forma íons, então não usa o fator de Vant’ Hoff: π = 0,1 . R . T
II. Sacarose 0,2 mol/L – molecular, não forma íons, então não usa o fator de Vant’ Hoff: π = 0,2 . R . T
III. 1 HCl → 1 H+ + 1 Cl-
π = M . R . T . i. → π = 0,1 . R . T . 2 → π = 0,2 . R . T
IV. 1 HCl → 1 H+ + 1 Cl-
π = M . R . T . i. → π = 0,2 . R . T . 2 → π = 0,4 . R . T
V. 1 NaOH → 1 Na+ + 1 OH-
π = M . R . T . i. → π = 0,1 . R . T . 2 → π = 0,2 . R . T
Assim, temos a seguinte ordem crescente de pressão osmótica:
Sacarose 0,1 mol/L < Sacarose 0,2 mol/L = HCl 0,1 mol/L = NaOH 0,1 mol/L< HCl 0,2 mol/L
(π = 0,1) (π = 0,2) (π = 0,2) (π = 0,2) (π = 0,4)
ou
I < II = III = V < IV.
Resposta Questão 4
Alternativa “d”.
Visto que é uma solução molecular, não é necessário considerar o fator de Van't Hoff (i). A temperatura deve ser dada na escala kelvin: 0ºC = 273 K.
π = M . R . T
π = 1,0 . 0,082 . 273
π = 22,4 atm.



