Questão 1
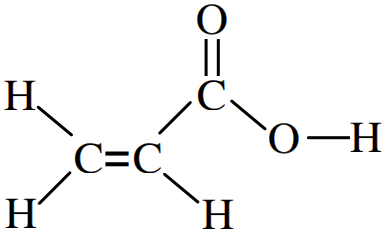
Analisando a fórmula estrutural da aspirina (princípio ativo muito utilizado para tratar dores de cabeça):
A quantidade de ligações pi existentes nela são:
a) 1
b) 2
c) 3
d) 4
e) 5
Questão 2
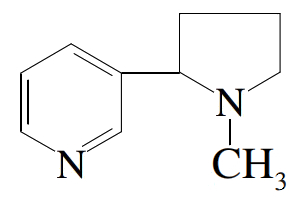
A nicotina, uma substância presente no cigarro e capaz de aumentar a frequência cardíaca, apresenta a seguinte estrutura:
Ela apresenta uma quantidade de ligações pi em carbonos secundários igual a:
a) 1
b) 2
c) 3
d) 4
e) 5
Questão 3
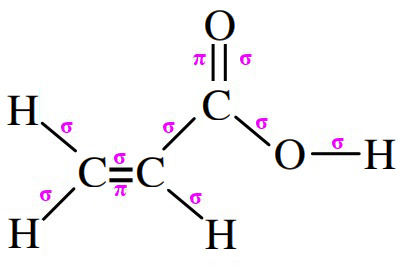
(UFF) As ligações químicas nos compostos orgânicos podem ser do tipo σ ou π. A ligação σ é formada pela interação de dois orbitais atômicos, segundo o eixo que une os dois átomos, ao passo que na ligação π, a interação dos orbitais atômicos se faz segundo o plano que contém o eixo da ligação.
Na estrutura representada acima, tem-se:
a) 2 ligações σ e 6 ligações π
b) 2 ligações σ e 8 ligações π
c) 4 ligações σ e 4 ligações π
d) 6 ligações σ e 2 ligações π
e) 8 ligações σ e 2 ligações π
Questão 4
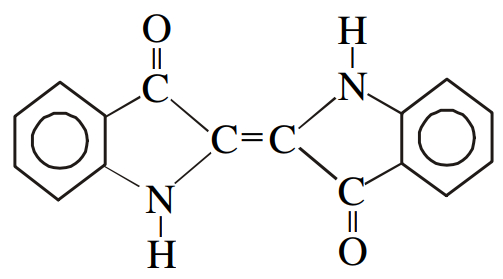
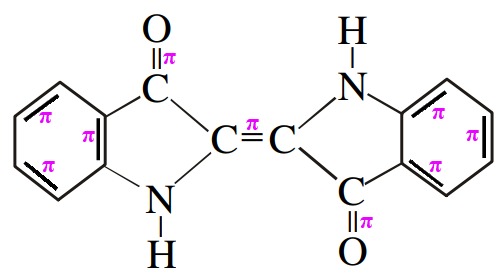
(UERJ) O tingimento na cor azul de tecidos de algodão com o corante índigo, feito com o produto natural ou com o obtido sinteticamente, foi o responsável pelo sucesso do jeans em vários países. Observe a estrutura desse corante:
Nessa substância, encontramos um número de ligações pi correspondente a:
a) 3
b) 6
c) 9
d) 12
Resposta Questão 1
Letra c). Toda ligação dupla (=) é formada por 1 ligação pi e 1 ligação sigma. Na estrutura da aspirina, existem 5 ligações duplas, logo, existem 3 ligações pi.
Resposta Questão 2
Letra b) Toda ligação dupla (=) é formada por 1 ligação pi e 1 ligação sigma. Na estrutura da nicotina, existem 3 ligações duplas, logo, existem 3 ligações pi. Porém, o exercício questiona quantas ligações pi estão localizadas em carbonos secundários – nesse caso, temos apenas duas (localizadas acima e à esquerda da primeira estrutura fechada).
Obs.: A ligação pi à direita da estrutura fechada está localizada no nitrogênio e em um carbono primário.
Resposta Questão 3
Letra e) Na ligação dupla, temos uma ligação sigma e outra pi. Como temos duas ligações duplas na estrutura, logo, ela apresenta 2 ligações pi. Já as ligações simples são ligações sigma. Como existem 6 ligações simples e mais 2 duplas, nesse ácido, há 8 ligações sigma.
Resposta Questão 4
Letra c) Sabe-se que em toda ligação dupla (=) existe 1 ligação pi e 1 ligação sigma. Na estrutura do corante, temos a presença de 9 delas, sendo 3 em cada um dos benzenos, 2 entre átomos de carbono e oxigênio e 1 entre átomos de carbono. Logo, ela apresenta 9 ligações pi.




.jpg)