Questão 1
Dadas as fórmulas moleculares das substâncias a seguir, indique aquela que apresente em sua constituição uma ou mais ligações covalentes dativas.
a) CO2
b) H2S
c) NH3
d) CO
e) HCN
Questão 2
O elemento químico enxofre está localizado na família VIA, ou família dos calcogênios, no terceiro período da tabela periódica. É um elemento químico formador de diversas substâncias, como o ácido sulfúrico (H2SO4), dióxido de enxofre (SO2) e o trióxido de enxofre (SO3). Qual é a quantidade de ligações covalentes dativas que esse elemento químico é capaz de realizar?
a) 6
b) 4
c) 2
d) 3
e) 1
Questão 3
(PUC-RJ) No composto P2O5, nas ligações P – O, o número de ligações covalentes dativas é:
a) 1
b) 2
c) 3
d) 4
e) 5
Questão 4
(ESAL-MG) O número máximo de ligações coordenadas ou dativas que o cloro pode efetuar é igual a:
a) 1
b) 2
c) 3
d) 4
e) 5
Resposta Questão 1
Letra d). A resposta é a alternativa d porque, para a realização de uma ligação dativa, é necessária a presença de um átomo instável e de outro que precise de dois elétrons. Assim, temos:
a- O carbono é o elemento que realiza o maior número de ligações, pois pertence à família IVA (possui 4 elétrons e precisa de 4 ligações), e fica posicionado no centro. Os dois oxigênios, que necessitam de 2 ligações cada por ser da família VIA, posicionam-se nas extremidades.
b- O enxofre é o elemento mais eletronegativo, pois é pertencente à família VIA (possui 6 elétrons e precisa de 2 ligações), e posiciona-se no centro. Os dois hidrogênios, que necessitam de apenas uma ligação cada, dispõem-se nas extremidades.
c- O nitrogênio é o elemento mais eletronegativo, pois é pertencente à família VA (possui 5 elétrons e precisa de 3 ligações), e posiciona-se no centro. Os três hidrogênios, que necessitam de apenas uma ligação cada, localizam-se nas extremidades.
d- A molécula apresenta um carbono, que pertence à família IVA (possui 4 elétrons e precisa de 4 ligações), e um átomo de oxigênio, que necessita de 2 ligações por ser da família VIA. O oxigênio estabiliza-se ao compartilhar dois elétrons com o carbono, porém o carbono não. Logo, temos um átomo estável e outro que necessita de 2 elétrons.
e- O carbono é o elemento que realiza o maior número de ligações por pertencer à família IVA (possui 4 elétrons e precisa de 4 ligações para estabilizar), e posiciona-se no centro da molécula. O hidrogênio, que necessita de uma ligação apenas, e o nitrogênio, que necessita de 3 ligações por ser da família VA, dispõem-se nas extremidades.
Resposta Questão 2
Letra c). Para determinar o número de ligações covalentes dativas que um elemento pode fazer, devemos conhecer sua camada de valência e o número de ligações covalentes normais que ele deve realizar para tornar-se estável. No caso do enxofre, temos:
- Camada de valência com 6 elétrons;
- Necessita compartilhar 2 de seus elétrons para tornar-se estável, ou seja, atingir 8 elétrons na camada de valência.
Assim, ao realizar duas ligações covalentes normais, sobram no enxofre quatro elétrons não ligantes. Como cada ligação dativa utiliza dois elétrons não ligantes do átomo estável, o enxofre pode fazer duas ligações dativas.
Resposta Questão 3
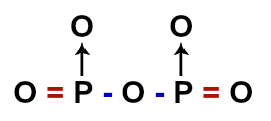
Letra b). A molécula apresenta ao todo 7 átomos: 2 de fósforo (capazes de realizar 3 ligações covalentes para estabilizar-se) e 5 oxigênios (capazes de realizar 2 ligações covalentes para estabilizar-se). Com esses dados, devemos montar a fórmula estrutural do composto para definir o número de ligações dativas presentes, seguindo o raciocínio abaixo:
1o Passo: Um dos átomos de oxigênio é posicionado no centro da molécula por ser mais eletronegativo. Ele media os dois átomos que fazem o maior número de ligações, que são os de fósforo. Assim, o centro da molécula apresenta três átomos:
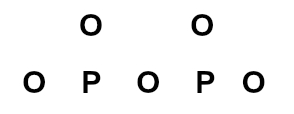
2o Passo: Em seguida, os outros átomos de oxigênio são posicionados nos polos (norte, sul ou leste) dos átomos de fósforo, o que resulta em dois oxigênios para cada fósforo:
3o Passo: Colocamos as ligações covalentes, começando da extremidade para o centro. Entre um oxigênio e o fósforo, colocamos uma ligação dupla, já que o oxigênio necessita de 2 ligações. Não podemos colocar outra dupla entre o outro oxigênio e o fósforo, pois o fósforo só faz 3 ligações:
4o Passo: Como o fósforo só precisa de mais uma ligação, ele realiza uma ligação simples com o oxigênio central.
5o Passo: Por fim, temos o oxigênio central estável, os dois átomos de fósforo estáveis e dois oxigênios nas extremidades estáveis, sobrando dois outros oxigênios que necessitam realizar duas ligações. Essas duas ligações que os oxigênios necessitam serão realizadas com o fósforo por meio de ligações dativas.
Resposta Questão 4
Letra c). O cloro é um elemento químico que pertence à família VIIA da tabela periódica, por isso, possui 7 elétrons na camada de valência. Assim, para estabilizar-se, ele deve realizar uma única ligação covalente simples, na qual utiliza um de seus sete elétrons para compartilhar, sobrando necessariamente 6 elétrons não ligantes.
Para a realização de uma ligação covalente dativa, o átomo deve apresentar um ou mais pares de elétrons não ligantes em sua camada de valência. Como o cloro possui 6 elétrons na camada de valência, então, possui três pares de elétrons não ligantes e pode realizar até 3 ligações covalentes dativas.




.jpg)
.jpg)
.jpg)
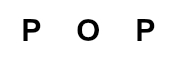
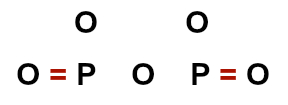
.jpg)