Questão 1
Dada a equação a seguir de uma determinada reação química:
H2O2 + 2 Cl- + 2 H3O+ → 2 H2O + Cl2
(Reagentes) (Produtos)
Foram realizados quatro experimentos com quantidades diferentes de reagentes. Em cada uma deles, foi medido o tempo que o Cl2 leva para ser originado. A tabela a seguir traz os dados desses experimentos:
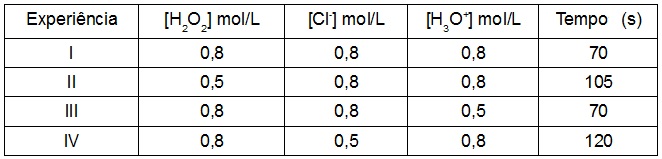
Esses dados indicam que a velocidade da reação considerada depende apenas da concentração de:
a) H2O2 e Cl-
b) H2O2 e H3O+
c) H2O2
d) H3O+
e) Cl-
Questão 2
Quando o ar de uma cidade está muito poluído, várias reações químicas podem ocorrer na atmosfera do local. Uma delas é a reação entre o dióxido de nitrogênio e o ozônio, que forma trióxido de nitrogênio e gás oxigênio, como na equação a seguir:
NO2(g) + O3(g) → NO3(g) + O2(g)
Utilizando os dados a seguir para a equação fornecida, determine a expressão da velocidade e o valor da constante da velocidade desse processo:
.jpg)
a) v = k · [NO2] e 2,2. 107
b) v = k · [O3] e 4,4. 107
c) v = k · [NO2] [O3] e 1,5. 107
d) v = k · [NO2] [O3] e 2,0. 107
e) v = k · [NO2] + [O3] e 2,2. 107
Questão 3
Dado o processo químico representado pela equação a seguir:
NO2 + CO → CO2 + NO
Sabe-se que o reagente monóxido de carbono não influi na velocidade da reação, mas o dióxido de nitrogênio, quando elevado ao quadrado, altera a velocidade. Sendo assim, marque a alternativa que fornece a equação da velocidade do processo:
a) v = k · [NO2]2
b) v = k · [CO3]
c) v = k · [NO2] [CO]
d) v = k · [NO2] [CO]
e) v = k · [NO2] + [CO]
Questão 4
(UFMT)
Dada a equação:
A + B → C
e o quadro cinético abaixo:
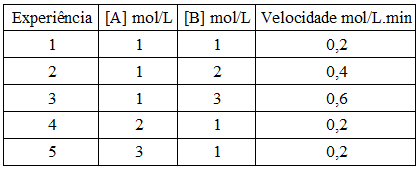
a expressão da velocidade que representa a reação é:
a) v = k . [A] [B]
b) v = k . [A]
c) v = k . [B]
d) v = k . [A] [B]2
e) v = k . [B]2
Questão 5
(ITA SP) Uma certa reação química é representada pela equação:
2A(g) + 2B(g) → C(g)
onde “A”, “B” e “C” significam as espécies químicas que são colocadas para reagir. Verificou-se experimentalmente, em uma certa temperatura, que a velocidade dessa reação quadruplica com a duplicação da concentração da espécie “A”, mas não depende das concentrações das espécies “B” e “C”. Assinale a opção que contém, respectivamente, a expressão CORRETA da velocidade e o valor CORRETO da ordem da reação.
a) v = k[A]2.[B]2 e 4
b) v = k[A]2.[B]2 e 3
c) v = k[A]2.[B]2 e 2
d) v = k[A]2 e 4
e) v = k[A]2 e 2
Questão 6
(IME)
A reação em fase gasosa
aA + bB → cC + dD
foi estudada em diferentes condições, tendo sido obtidos os seguintes resultados experimentais:
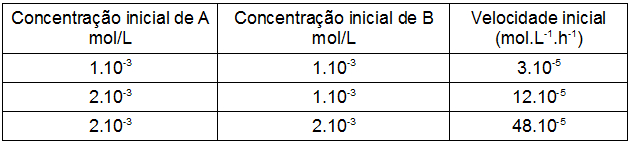
A partir dos dados acima, determine a constante de velocidade da reação.
Resposta Questão 1
Letra a). Analisando o experimento II e III, percebemos que a quantidade de H2O2 e de H+, respectivamente, muda e o tempo também. Já no experimento IV, percebemos que a quantidade do I- mudou, mas o tempo não (manteve o mesmo padrão de tempo do experimento I quando todos tinham a mesma concentração).
Resposta Questão 2
Letra c). Para determinar a constante de velocidade, é necessário formular a expressão da velocidade. Para isso, temos que descobrir a ordem de cada um dos participantes reagentes da equação.
v = K.[NO2]a.[O3]b
Ordem do participante NO2:
Vamos escolher a segunda e a terceira filas horizontais da tabela porque nelas a concentração de O3 não sofre alteração e a de NO2, sim. Da segunda para terceira, a concentração de NO2 passa de 15.10-5 para 7,5.10-5, isto é, reduziu pela metade. Já a velocidade passa de 13,2.10-2 para 6,6.10-6, também reduzindo pela metade. Assim:
[NO2] = 15.10-5 para 7,5.10-5 v = 13,2.10-2 para 6,6.10-6
[NO2] = 1/2 v = 1/2
Como a redução da concentração e a da velocidade foram as mesmas, a ordem para o participante NO2 é 1.
Ordem do participante O3
Para a ordem do O3, vamos escolher a primeira e segunda filas horizontais da tabela, já que nelas a concentração de NO2 não sofreu alteração e a de O3, sim. Da primeira para a segunda, a concentração de O3 passou de 3.10-5 para 6.10-5, ou seja, dobrou. Já a velocidade passou de 6,6.10-2 para 13,2.10-2, também dobrou. Assim:
[O3] = 3.10-5 para 6.10-5 v = 6,6.10-6 para 13,2.10-2
[O3] = 2 v = 2
Como o aumento da concentração e o da velocidade foram os mesmos, a ordem para o participante O2 é 1.
Conhecendo as ordens, a equação da velocidade será:
v = K.[NO2]1.[O3]1
Para calcular a constante da velocidade, basta utilizar os dados de qualquer uma das três linhas horizontais. Vamos utilizar a primeira:
6,6.10-2 = K.[15.10-5].[3.10-5]
6,6.10-2 = K.4510-10
6,6.10-2 = K. 4510-10
K = 6,6.10-2
45.10-10
K = 1,5 .107 mol-.L.h-1
Resposta Questão 3
Letra a). Como o participante CO não influi na velocidade, sua ordem é 0; assim, ele não aparece na equação da velocidade. Já o participante NO2 terá sua concentração elevada a 2 como indicado no enunciado.
Resposta Questão 4
Letra c). Para determinar a constante de velocidade, é necessário formular a expressão da velocidade. Para isso, temos que descobrir a ordem de cada um dos participantes reagentes da equação.
v = K.[A]a.[B]b
Ordem do participante B:
Vamos escolher a primeira e a segunda filas horizontais porque nelas a concentração de B não sofre alteração e a de A, sim. Da primeira para a segunda, a concentração de B passou de 1 para 2, ou seja, dobrou. Já a velocidade passou de 0,2 para 0,4, também dobrou. Assim:
[B] = 1 para 2 v = 0,2 a 0,4
[B] = 2 v = 2
Como o aumento na concentração e na velocidade são iguais, a ordem para o participante B é 1.
Ordem do participante A
Vamos escolher a primeira e quarta filas horizontais porque nelas a concentração de B não sofre alteração e a de A, sim. Da primeira para a quarta, a concentração de A passou de 1 para 2, ou seja, dobrou. Já a velocidade não sofreu nenhuma alteração.
[B] = 1 para 2 v = 0,2 a 0,2
[B] = 2 v = 0
Como o participante não influi na velocidade, sua ordem é 0.
Como apenas o participante B participa da reação, com ordem 1, sua expressão da velocidade é enunciada da seguinte forma:
v = k . [B]
Resposta Questão 5
Letra e). Para começar a resolução desse exercício, devemos entender quais foram os dados fornecidos por ele:
-
A velocidade da reação quadruplica quando A é duplicado: 4v quando 2.[ ].
-
A concentração de B e C não influenciam o valor da reação e, por isso, a ordem de cada um é igual a 0.
Além disso, o reagente B não apresenta nenhuma influência na velocidade da reação e, por isso, sua ordem é 0. De acordo com o enunciado, a velocidade de A duplica, indicando que sua ordem é 2. Como A está só na equação da velocidade, a ordem da reação é 2 e a equação da velocidade é: v = k[A]2.
Resposta Questão 6
Para determinar a constante de velocidade, é necessário formular a expressão da velocidade. Para isso, temos que descobrir a ordem de cada um dos participantes reagentes da equação.
v = K.[A]a.[B]b
Ordem do participante A:
Vamos escolher a primeira e a segunda filas horizontais porque nelas a concentração de B não sofre alteração, e, sim, a de A. Da primeira para a segunda fila, a concentração de A passou de 1.10-3 para 2.10-3, ou seja, dobrou, e a velocidade passou de 3.10-5 e 12.10-5, isto é, quadruplicou. Assim:
[A] = 1.10-3 para 2.10-3 v = 3.10-5 para 12.10-5
[A] = 2 v = 4
Relacionando a concentração com a velocidade, temos que a relação entre elas é igual a 2; logo, a ordem para o participante A é 2.
Ordem do participante B:
Vamos escolher a segunda e a terceiras filas horizontais porque nelas a concentração de A não sofre alteração, e, sim, a de B. Da segunda para a terceira, a concentração de A passou de 1.10-3 para 2.10-3, ou seja, dobrou, e a velocidade passou de 12.10-5 à 48.10-5, quadruplicou.
[B] = 1.10-3 para 2.10-3 v = 12.10-5 à 48.10-5
[B] = 2 v = 4
Relacionando a concentração com a velocidade, temos que a relação entre elas é igual a 2; logo, a ordem para o participante B é 2.
Conhecendo as ordens, temos que a equação da velocidade é:
v = K.[A]2.[B]2
Para calcular a constante da velocidade, basta utilizar os dados de qualquer uma das três linhas horizontais. Vamos utilizar a primeira:
3.10-5 = K.[1.10-3]2.[1.10-3]2
3.10-5 = K. 10-6. 10-6
3.10-5 = K. 10-12
K = 3.10-5
10-12
K = 3 .107 mol-3.L3.h-1



