Questão 1
(UESPI) Qualquer que seja a procedência ou processo de preparação do NaCl, podemos afirmar que sua composição é sempre 39,32% de sódio e 60,68% de cloro, com base na lei de:
a) Lavoisier
b) Dalton
c) Proust
d) Richter
e) Avogadro
Questão 2
(Vunesp) Foram analisadas três amostras (I, II e III) de óxidos de enxofre, procedentes de fontes
distintas, obtendo-se os seguintes resultados:
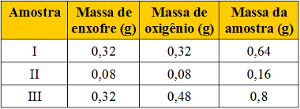
Tabela com dados em exercícios sobre a lei de Proust
Esses resultados mostram que:
a) as amostras I, II e III são do mesmo óxido.
b) apenas as amostras I e II são do mesmo óxido.
c) apenas as amostras II e III são do mesmo óxido.
d) apenas as amostras I e III são do mesmo óxido.
e) as amostras I, II e III são de óxidos diferentes.
Questão 3
Observe na tabela a seguir as massas dos reagentes e do produto de uma reação que foram obtidas em várias experiências:

Tabela com dados em exercício sobre a lei das proporções constantes de Proust
Baseado na lei das proporções constantes de Proust, determine os valores de A, B, C, D, E e F, respectivamente:
a) 56g, 68g, 3g, 17g, 6g, 11g
b) 34g, 46g, 20g, 34g, 28g, 5g
c) 56g, 34g, 6g, 34g, 28g, 11g
d)34g, 68g, 3g, 34g, 6g, 11g
e) 46g, 58g, 3g, 17g, 6g, 11g
Questão 4
É possível diminuir a acidez do suco de limão adicionando-se a ele uma pequena quantidade de bicarbonato de sódio. A reação que ocorre e que justifica essa diminuição de acidez é apresentada a seguir:
Ácido + Bicarbonato → citrato + água + dióxido de
cítrico de sódio de sódio carbono
Para uma total neutralização, são necessários 252 g de bicarbonato de sódio para 192 g de ácido cítrico. Qual é a massa de bicarbonato de sódio necessária para neutralizar 0,96 g de ácido cítrico presente em uma limonada?
a) 252 g.
b) 0,192 g.
c) 2,35 g.
d) 1,92 g.
e) 1,26 g.
Resposta Questão 2
Alternativa “b”.
Observe qua as amostras I e II seguem a lei de Proust e mantêm a proporção da reação constante. Da amostra I para a II, a massa de todos os participantes na reação diminuiu exatamente ¼. Já a amotra III não manteve a proporção
Resposta Questão 3
Alternativa “a”.
A lei de Proust diz que a proporção em massa das substâncias que reagem e que são produzidas em uma reação é fixa, constante e invariável. Assim, se a primeira reação segue a seguinte proporção em massa 28 : 6 : 34 , essa proporção deve continuar a ser seguida, veja:
* II – A + 12 g → B
O valor da massa de H2 dobrou de 6 g para 12 g, então as massas das outras substâncias também devem dobrar:
II – 56 g + 12 g → 68 g
*III – 14 g + C → D
O valor da massa de N2 diminuiu pela metade, de 28 g para 14 g, então as massas das outras substâncias também devem diminuir pela metade:
III – 14 g + 3 g → 17 g
*IV – 56 g + E → 34 g + 28 g de N2
Veja que a massa de N2 dobrou (de 28 g para 56 g), no entanto, esse valor que aumentou ficou em excesso e sobrou no final, o que significa que a massa do H2 permaneceu constante em 6 g e reagiu completamente com 28 g de N2.
IV – 56 g + 6 g → 34 g + 28 g de N2
*V – 28 g + F → 34 g + 5 g de H2
Observe que a massa de N2 continuou a mesma, mas como sobraram 5 g de H2, isso quer dizer que esse valor estava em excesso. Assim, foram acrescentados 5 g de H2 aos 6 g que já havia, ficando 11 g:
V – 28 g + 11 g → 34 g + 5 g de H2
Resposta Questão 4
Alternativa “e”.
Seguindo a lei das proporções constantes de Proust, temos:
192 g de ácido cítrico ----- 252 g de bicarbonato de sódio
0,96 g de ácido cítrico ---- x
x = 0,96 . 252
192
x = 1,26 g



