Questão 1
Sabe-se que a isomeria geométrica cis-trans está presente em cadeias abertas insaturadas (que contêm uma ligação dupla), ou em uma estrutura saturada cíclica, desde que apresentem dois ligantes diferentes em cada carbono da dupla ou em dois dos carbonos do ciclo, sendo esses ligantes iguais entre si. No caso da isomeria geométrica E-Z, a diferença está:
a) No raio atômico dos átomos ligados aos carbonos da dupla ou aos dois carbonos do ciclo.
b) Na maior eletronegatividade dos átomos ligados aos carbonos da dupla ou aos dois carbonos do ciclo.
c) Na maior massa atômica dos átomos ligados aos carbonos da dupla ou aos dois carbonos do ciclo.
d) No maior número atômico dos átomos ligados aos carbonos da dupla ou aos dois carbonos do ciclo.
e) Na maior energia de ionização dos átomos ligados aos carbonos da dupla ou aos dois carbonos do ciclo.
Questão 2
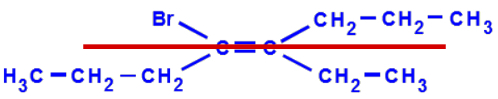
Assinale a alternativa que fornece o nome do composto orgânico cuja fórmula encontra-se esquematizada a seguir:
a) cis-4-bromo-5-etil-4-octeno.
b) E-4-bromo-5-etil-4-octeno.
c) trans-4-bromo-5-etil-4-octeno.
d) Z-4-bromo-5-etil-4-octeno.
e) Z-4-etil-5-bromo-4-octeno.
Questão 3
Admite isomeria geométrica E-Z o alceno de nome:
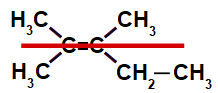
a) 2,3-dimetil-pent-2-eno.
b) Pent-1-eno.
c) 3-metil-hex-3-eno.
d) Eteno.
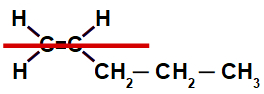
e) Hex-3-eno.
Questão 4
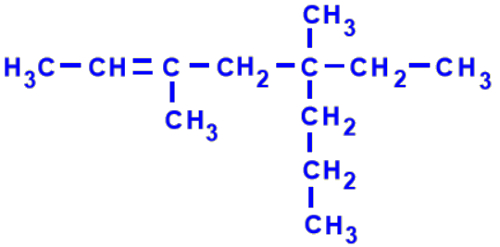
Em relação ao composto a seguir, são feitas as seguintes afirmações:
I. É um composto que apresenta isomeria cis-trans.
II. É um composto que apresenta isomeria E-Z.
III. Seu nome IUPAC é 3, 5 dimetil–3– propil–hept-5-eno.
IV. Apresenta somente uma ligação pi.
São corretas, apenas, as afirmações:
a) IV.
b) I e II.
c) I.
d) II e IV.
e) I e III.
Resposta Questão 1
Letra d). A isomeria geométrica do tipo E-Z utiliza como pontos de análise o número atômico dos átomos ligados aos carbonos da dupla ou aos dois carbonos do ciclo, além do tamanho dos radicais orgânicos ligados a esses carbonos.
Resposta Questão 2
Letra e). Esse haleto apresenta isomeria geométrica E-Z, pois os ligantes dos carbonos da dupla ligação são diferentes entre si, com exceção do radical propil (H3C-CH2-CH2).
Quando passamos o plano central dividindo a cadeia em plano superior e inferior, observamos que o ligante de maior número atômico (Br), do carbono à esquerda da dupla, está no mesmo plano que o maior radical do carbono à direita da dupla. Logo, verifica-se um isômero Z.
Em um haleto orgânico, devemos iniciar a numeração da cadeia sempre pela extremidade mais próxima de uma ramificação (H3C-CH2), e não no halogênio (Br).
Resposta Questão 3
Letra c). Para encontrar a resposta desse exercício, devemos analisar a fórmula estrutural de cada um dos compostos que apresenta um plano:
a- Falso. Esse composto não apresenta isomeria geométrica, pois apresenta dois ligantes iguais no carbono à esquerda da dupla:
b- Falso. Esse composto não apresenta isomeria geométrica, pois apresenta dois ligantes iguais no carbono à esquerda da dupla:
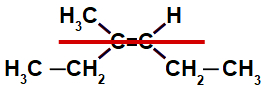
c- Verdadeiro. Os ligantes dos carbonos da dupla não são iguais entre si, com exceção do radical etil (H3C-CH2):
d- Falso. O composto não apresenta isomeria geométrica, pois apresenta dois ligantes iguais nos carbonos da dupla:
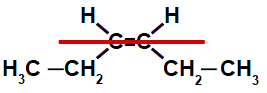
e- Falso. Esse composto apresenta isomeria geométrica cis-trans e os mesmos ligantes em ambos carbonos da dupla:
Resposta Questão 4
Letra d).
I- Falso. Para apresentar isomeria geométrica cis-trans, os ligantes de ambos os carbonos da dupla devem ser iguais.
II- Verdadeiro. Os ligantes dos carbonos da dupla não são iguais entre si, com exceção do radical metil (H3C-).
III- A nomenclatura está incorreta porque a cadeia principal de um alceno apresenta os carbonos da dupla e o maior número de carbonos possível. No caso dessa estrutura, a cadeia principal apresenta oito carbonos (prefixo oct).
IV- Verdadeiro. A estrutura apresenta apenas uma ligação dupla, portanto, possui uma ligação pi.




.jpg)
.jpg)
.jpg)