Questão 1
(UECE) Considere os seguintes ácidos com seus respectivos graus de ionização (a 18oC) e usos:
I. H3PO4 (α = 27%), usado na preparação de fertilizantes e como acidulante em bebidas e refrigerantes.
II. H2S (α = 7,6 . 10-2 %), usado como redutor.
III. HClO4 (α = 97%), usado na Medicina, em análises químicas e como catalisador em explosivos.
IV. HCN (α = 8,0 . 10-3 %), usado na fabricação de plásticos, corantes e fumigantes para orquídeas e poda de árvores.
Podemos afirmar que são corretas:
a) HClO4 e HCN são ácidos fracos
b) H3PO4 e H2S são ácidos fortes
c) H3PO4 é considerado um ácido semiforte
d) H2S é um ácido semiforte
e) n.d.a
Questão 2
(FCB-Araras-SP) Após a ionização de um ácido em água, observou-se que o número de moléculas ionizadas era o quádruplo do número de moléculas não ionizadas. Com base nessa observação, a porcentagem de ionização do referido ácido era:
a) 26%
b) 40%
c) 70%
d) 75%
e) 80%
Questão 3
Dados os ácidos a seguir e seus respectivos graus de ionização, indique a alternativa que apresenta a ordem crescente de força entre eles:
Determine a ordem de acidez dos seguintes compostos:
I. HNO3 (α = 92 %)
II. H2S (α = 0,076 %)
III. H3PO4 (α = 27 %)
IV. H2SO4 (α = 61 %)
a) II>III>IV>I
b) III>IV>I>II
c) I>III>IV>II
d) I>II>III>IV
e) I>IV>III>II
Questão 4
Quanto maior a força de um ácido, maior é sua capacidade de sofrer ionização e, consequentemente, produzir íons em água. Assim, é possível acender uma lâmpada utilizando apenas uma cuba de vidro, dois fios elétricos e um soquete. Qual dos ácidos abaixo, ao ser adicionado à água, seria capaz de ionizar-se bastante e, com isso, acender a lâmpada com um brilho mais intenso?
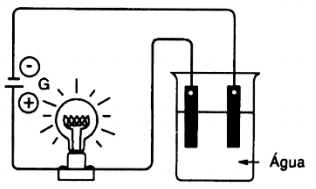
a) HF (α = 8 %)
b) H2S (α = 0,076 %)
c) H3PO4 (α = 27 %)
d) H4SiO4 (α ?< 5 %)
e) HNO3 (α = 92 %)
Resposta Questão 1
Letra c). A letra “c” está correta porque, se o ácido apresenta seu grau de ionização entre 5 e 50%, ele é considerado semiforte. A letra “a” está errada porque o HClO4 é um ácido forte, já que apresenta grau de ionização maior que 50 %. A letra “b” está incorreta porque os dois ácidos em questão (H3PO4 e H2S) não podem ser fortes por apresentarem grau de ionização menor que 50 %. A letra “d” está incorreta porque, como o H2S possui um grau de ionização menor que 5%, ele é um ácido fraco.
Resposta Questão 2
Letra e). Os dados fornecidos pelo exercício foram:
no de partículas ionizadas = X (APENAS INFORMA QUE ELAS SÃO O QUÁDRUPLO DAS NÃO IONIZADAS)
no de partículas não ionizadas = Y (NÃO FOI INFORMADO)
no de partículas total = Z (É a SOMA DE X + Y)
Como a questão informa que o número de moléculas ionizadas é quatro vezes maior que o número de moléculas não ionizadas, logo:
X = 4.Y ou Y = X
4
O número total de partículas é soma das ionizadas com as não ionizadas. Como estamos falando de ionização, substituiremos no lugar de Y a expressão X/4, já que X é o número de partículas ionizadas. Assim:
Z = X + Y
Z = X + X
4
Z = 5X
4
Para encontrar a porcentagem de ionização, basta utilizar a fórmula do cálculo do grau de ionização (α):
α = no de partículas ionizadas
no de partículas total
α = X
5X/4
α = 4X
5X
α = 0,8 ou 80 %
Resposta Questão 3
Letra e). Se o ácido apresenta grau de ionização maior ou igual a 50 %, ele é forte, logo os ácidos HNO3 e H2SO4 são fortes. Todavia HNO3 (I) é mais forte por ter maior grau de ionização. O H3PO4 (III) é um ácido semiforte por ter um grau de ionização entre 50 e 5 %. Já o H2S (II) é um ácido fraco por ter grau de ionização menor que 5%.
Resposta Questão 4
Letra e). Quanto maior o grau de ionização, mais forte é o ácido. Dessa forma, o ácido que, ao se ionizar, favorecerá um brilho mais intenso à lampada é o ácido cujo grau de ionização ultrapassa o valor de 50%, que é o HNO3.



