Questão 1
Os gases ideais podem sofrer transformações nas quais seu volume permanece constante. De acordo com seus conhecimentos sobre as transformações isovolumétricas, assinale a alternativa CORRETA:
a) Nas transformações isovolumétricas, a pressão do gás permanece constante.
b) Nas transformações isovolumétricas, a energia interna do gás permanece inalterada.
c) Nas transformações isovolumétricas, o gás não realiza trabalho.
d) Nas transformações isovolumétricas, a energia interna do gás sempre aumenta.
e) Nas transformações isovolumétricas, a energia interna do gás sempre diminui.
Questão 2
Com base em seus conhecimentos sobre as transformações isovolumétricas e sobre a primeira lei da Termodinâmica, pode-se afirmar que:
a) nas transformações isovolumétricas, a realização de trabalho pelo ou sobre o gás é positiva. Dessa forma, a variação da energia interna do gás é igual à quantidade de calor absorvida ou emitida por ele.
b) nas transformações isovolumétricas, a realização de trabalho pelo ou sobre o gás é nula. Dessa forma, a variação da energia interna do gás é igual à quantidade de calor absorvida ou emitida por ele.
c) nas transformações isovolumétricas, a realização de trabalho pelo ou sobre o gás é negativa. Dessa forma, a variação da energia interna do gás é igual à quantidade de calor absorvida ou emitida por ele.
d) nas transformações isovolumétricas, o gás sempre sofrerá incrementos em sua energia interna.
e) se um gás sofrer uma transformação isovolumétrica na qual sua pressão aumente, o trabalho terá sido realizado sobre o gás.
Questão 3
Durante uma transformação isovolumétrica, um gás ideal monoatômico cede 40 J de calor para o meio externo. A variação da energia interna do gás e o trabalho realizado na transformação são, respectivamente, iguais a:
a) ΔU = - 40 J; τ = 0 J
b) ΔU = 0 J; τ = - 40 J
c) ΔU = 0 J; τ = 40 J
d) ΔU = 40 J; τ = 0 J
e) ΔU = 40 J; τ = 40 J
Questão 4
Um gás ideal sofre uma transformação termodinâmica AB, representada no gráfico abaixo:
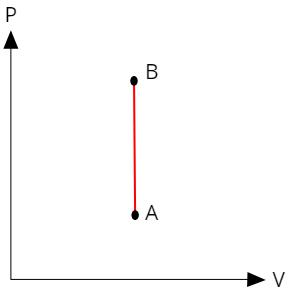
Assinale a alternativa verdadeira em relação a essa transformação.
a) A transformação sofrida pelo gás é adiabática.
b) A transformação sofrida pelo gás é isotérmica.
c) A transformação sofrida pelo gás é isobárica.
d) A transformação sofrida pelo gás é isovolumétrica.
Questão 5
A primeira lei da Termodinâmica aplica-se a quaisquer transformações sofridas por um sistema fechado. De acordo com essa lei, durante uma transformação que ocorra em um recipiente de paredes rígidas, é correto afirmar que:
a) o trabalho realizado é positivo, quando realizado pelo sistema.
b) o trabalho total realizado sobre ou pelo sistema é nulo.
c) o trabalho realizado é negativo, quando realizado sobre o sistema.
d) não ocorrerão trocas de calor em razão das características das paredes do recipiente.
e) não haverá mudança de temperatura.
Questão 6
Algumas transformações especiais sofridas pelos gases ideais são descritas por leis físicas. A lei dos gases que explica o comportamento das transformações físicas que ocorrem em recipientes rígidos e fechados é conhecida como:
a) lei de Clapeyron
b) lei de Charles
c) lei de Boyle-Mariotte
d) lei de Gay-Lussac
e) lei de Newton
Questão 7
Durante uma transformação isovolumétrica, um gás ideal sofre um aumento em sua pressão, tendo-a triplicada. Sendo a temperatura inicial do gás igual a 473 ºC, determine a sua temperatura final, em ºC.
a) 0,05 di
b) 20 di
c) 5 di
d) 0,2 di
e) 3 di
Questão 8
Durante uma transformação isocórica, um gás dioatômico ideal teve a sua energia interna aumentada em 400 cal. Determine a quantidade de calor que esse gás absorveu durante o processo.
a) -400 cal
b) 400 cal
c) 800 cal
d) -800 cal
e) 200 cal
Resposta Questão 1
Letra C
a) FALSA – um exemplo de transformação isovolumétrica é aquela que acontece dentro de uma panela de pressão. Nesse caso, mantendo-se o volume constante, a pressão do gás tende a aumentar.
b) FALSA – nas transformações isovolumétricas, a temperatura do gás pode mudar, alterando, assim, sua energia interna.
c) VERDADEIRA – se o gás não muda de volume, não há realização de trabalho.
d) FALSA – se a temperatura do gás diminuir, sua energia interna também diminuirá.
e) FALSA - se a temperatura do gás aumentar, sua energia interna também aumentará.
Resposta Questão 2
Letra B
Nas transformações isovolumétricas, a realização de trabalho pelo ou sobre o gás é nula. Dessa forma, a variação da energia interna do gás é igual à quantidade de calor absorvida ou emitida pelo gás. Podemos constatar a veracidade dessa afirmação por meio da primeira lei da Termodinâmica:
![]()
Para uma transformação isovolumétrica, a quantidade de trabalho é nula. Logo:
![]()
Resposta Questão 3
Letra A
A primeira lei da Termodinâmica para transformações isovolumétricas é dada pela equação abaixo:
![]()
Como o gás cede calor para o meio externo, sua variação de energia interna é negativa, pois
ΔU = Q = - 40 J. Além disso, nas transformações isovolumétricas, o trabalho é sempre nulo, de forma que τ = 0 J.
Resposta Questão 4
Letra D
É possível perceber pelo gráfico que, durante a transformação AB, o gás não sofre alterações em seu volume. Podemos dizer, portanto, que o gás sofre uma transformação isovolumétrica.
Resposta Questão 5
Letra B
O processo descrito no enunciado do exercício ocorre ao volume constante, logo, trata-se de uma transformação isovolumétrica. Nesse tipo de transformação, como não há aumento ou diminuição do sistema, não há realização de trabalho. Portanto, em quaisquer processos físicos com essa característica, o trabalho total realizado deve ser nulo. Dessa forma, a alternativa correta é letra B.
Resposta Questão 6
Letra D
A lei física que explica o comportamento dos gases ideais em transformações isocóricas (a volume constante) é conhecida como lei de Gay-Lussac. Essa lei afirma que a razão entre pressão e temperatura de um gás ideal, antes e depois de uma transformação isovolumétrica, deve ser mantida de forma constante. Portanto, a alternativa correta é a letra D.
Resposta Questão 7
Letra C
Para resolvermos o exercício, devemos fazer o cálculo usando a lei de Gay-Lussac para processos isovolumétricos. Para tanto, é necessário lembrar que a pressão do gás ao final do processo é três vezes sua pressão inicial (PF = 3P0). Além disso, precisamos fazer o cálculo usando a temperatura em Kelvin (TK = TC – 273), que resulta em uma temperatura inicial de 200 K. Tomando os dados do enunciado, é preciso resolver o seguinte cálculo:
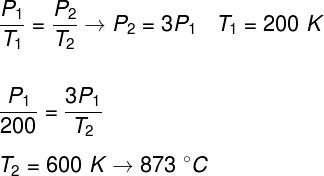
Resposta Questão 8
Letra B
A primeira lei da Termodinâmica para os processos isovolumétricos sofridos por gases ideais é dada pela equação a seguir:
![]()
Como a variação da energia interna do gás foi positiva, então a quantidade de calor por ele absorvida também foi positiva, logo, sua variação de energia interna foi de + 400 cal. A informação que diz respeito à conformação do gás diatômica poderia ser utilizada caso o exercício pedisse para que calculássemos a variação de temperatura sofrida por esse gás. Portanto, a alternativa correta é a letra B.



