Questão 1
Assinale a alternativa que apresenta a unidade de medida de entropia, de acordo com o Sistema Internacional de Unidades:
a) cal/ºC
b) J/K
c) cal/J
d) W/m
e) cal/gºC
Questão 2
Durante um processo espontâneo, podemos afirmar que a entropia de um sistema termodinâmico:
a) sempre diminui.
b) permanece constante.
c) aumenta até um valor máximo.
d) diminui até chegar a zero.
e) aumenta e depois diminui até chegar a zero.
Questão 3
Durante uma transformação reversível e isotérmica a 25 ºC, a variação de entropia de um sistema termodinâmico foi de 20 cal/ºC. Determine a quantidade de calor trocada entre o sistema e o meio externo.
a) 0,8 cal
b) 0,25 cal
c) 500 cal
d) 20 cal
e) 30 cal
Questão 4
À medida que a entropia de um sistema termodinâmico aumenta:
a) seu grau de aleatoriedade diminui à mesma medida.
b) sua temperatura aumenta.
c) sua pressão diminui.
d) seu grau de aleatoriedade aumenta à mesma medida.
e) sua energia interna aumenta à mesma medida.
Resposta Questão 1
Letra B
Como a entropia é dada pela razão do calor transferido na transformação isotérmica pela temperatura absoluta, sua unidade, de acordo com o Sistema Internacional de Unidades, é o Joule por Kelvin (J/K).
Resposta Questão 2
Letra C
Em todo processo espontâneo, há somente aumento da entropia. Nesses processos os sistemas sempre aumentam o seu grau de aleatoriedade. Nos processos reversíveis, entretanto, a entropia permanece constante.
Resposta Questão 3
Letra C
Para calcularmos a quantidade de calor transferida durante esse processo, utilizamos a seguinte fórmula:
![]()
Tomando os dados fornecidos pelo enunciado do exercício, faremos o seguinte cálculo:
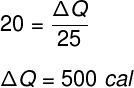
Resposta Questão 4
Letra D
Junto ao aumento de entropia em um sistema termodinâmico, também ocorre o aumento do grau de aleatoriedade de um sistema, portanto, a alternativa correta é a letra D.



